

在人类细胞的精密运作中,蛋白质的功能严格受制于其亚细胞定位。以端粒酶逆转录酶(hTERT)为例,这一关键蛋白在核内负责维持端粒长度,赋予癌细胞无限增殖的能力;而在线粒体中,它则通过增强呼吸链功能、清除活性氧(ROS)来提升癌细胞的应激抗性,呈现出截然不同的“双重身份”。然而,由于hTERT主要锚定于细胞核,传统药物难以有效干预其在不同区室的功能。针对这一难题,本研究提出了一种全新的干预策略:通过在活细胞内主动调控hTERT的运输路径,将其“禁锢”于非功能区域,旨在同时从时空维度瓦解其促癌机制。
91直播-美女直播-性爱直播 仰大勇教授与天津大学姚池教授合作,开发了一种能够在活细胞内执行“识别—组装—传感—调控”一体化功能的可编程DNA纳米系统,实现了对hTERT的特异性识别响应、空间限域与转运过程的动态调控,并同步输出多层次生物信号,为活细胞内的蛋白质功能研究与肿瘤精准干预提供了智能化的新工具。该成果发表在《德国应用91直播 》期刊(Angew. Chem. Int. Ed.2026, 65, e25891)。
受天然细胞区室化调控机制的启发,研究团队构建了一种基于枝状DNA(S-T-DNA)的动态自组装系统。该系统通过模块化设计整合了线粒体靶向单元三苯基膦(TPP)、端粒酶识别引物以及自组装回文序列,实现了在肿瘤细胞内的特异性激活与程序化组装。进入肿瘤细胞后,其端粒酶识别模块可特异性响应肿瘤标志物hTERT蛋白,触发链置换反应释放功能基元,进而在胞质中动态组装为靶向线粒体的DNA凝聚体。该过程可通过荧光共振能量转移实现实时原位监测,从而在活细胞内实现对人工纳米结构组装与演变的可视化追踪。形成的DNA凝聚体不仅作为功能执行单元,也构成一个集成的生物传感界面:通过扰动线粒体膜电位并诱导活性氧水平升高,直观反馈对细胞器的影响;升高的活性氧进一步作为信号,驱动hTERT蛋白从核内向胞质转位。借助荧光共定位与蛋白质定量分析,揭示了hTERT被捕获并滞留于DNA凝聚体的过程,实现了对目标蛋白迁移行为的动态示踪。研究结果表明,该系统可有效抑制hTERT功能,导致肿瘤细胞端粒缩短、线粒体DNA损伤及增殖显著受阻。
该工作推动了DNA纳米技术从静态结构设计向动态生命系统调控的跨越,为发展兼具实时传感与精准干预功能的肿瘤诊疗新模式奠定了基础。
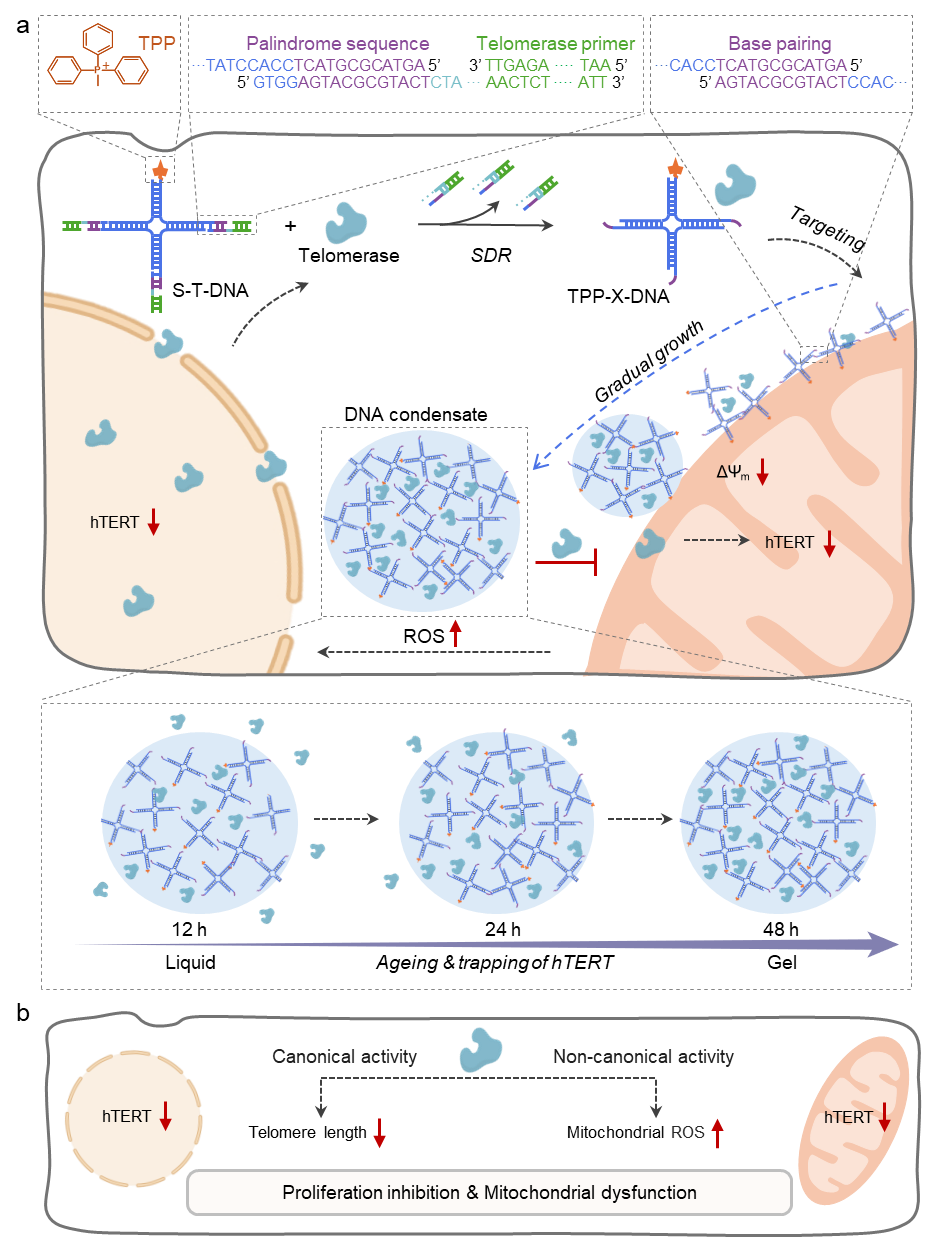
图1.可编程DNA凝聚体在活细胞内动态响应肿瘤标志物hTERT蛋白,实现“识别—组装—传感—调控”一体化,动态调控hTERT空间限域与转运过程,并同步输出多层次生物信号。
联系我们
社交媒体
版权所有 © 91直播-美女直播-性爱直播 2024 技术支持:维程互联





